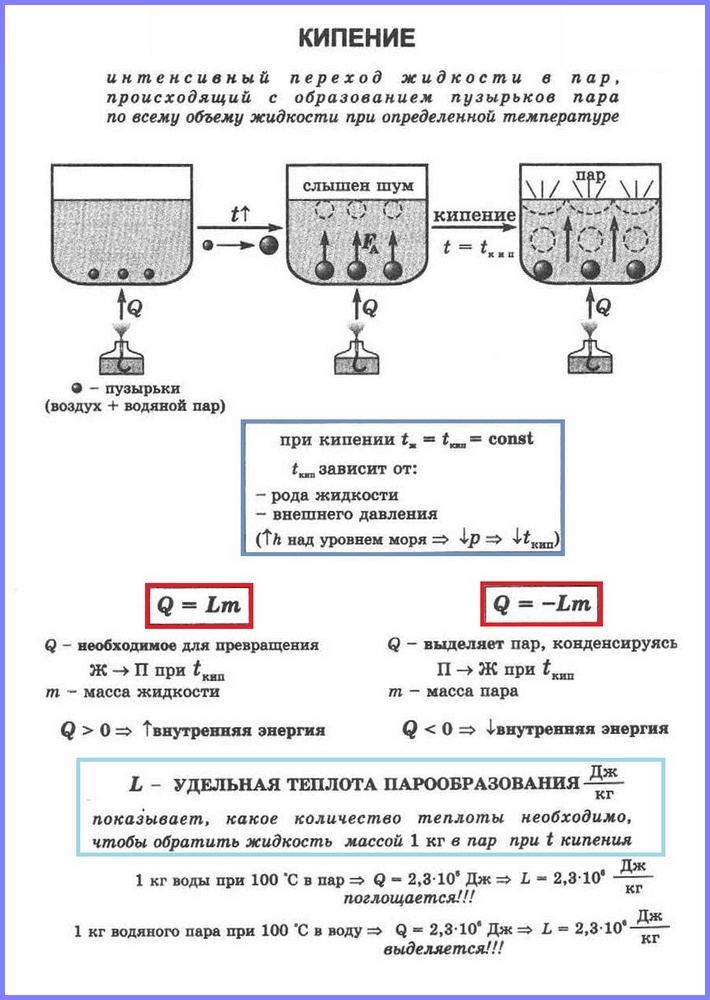
Знаете ли вы, какова температура варящегося супа? 100 ˚С. Ни больше, ни меньше. При той же температуре закипает чайник, и варятся макароны. Что это значит?
Почему при постоянном подогреве кастрюльки или чайника горящим газом температура воды внутри не подымается выше ста градусов? Дело в том, что когда вода достигает температуры в сто градусов, вся поступающая тепловая энергия расходуется на переход воды в газообразное состояние, то есть испарение. До ста градусов испарение происходит в основном с поверхности, а достигнув этой температуры, вода закипает. Кипение - это тоже испарение, но только по всему объему жидкости. Пузырьки с горячим паром образуются внутри воды и, будучи легче воды, эти пузырьки вырываются на поверхность, а пар из них улетучивается в воздух.
До ста градусов температура воды при нагревании растет. После ста градусов при дальнейшем нагревании будет расти температура водяного пара. А вот пока вся вода не выкипит при ста градусах, ее температура не повысится, сколько энергии не прикладывай. Куда девается эта энергия, мы уже разобрались - на переход воды в газообразное состояние. Но раз существует такое явление, значит должна быть описывающая это явление физическая величина. И такая величина существует. Называется она удельной теплотой парообразования.
Удельная теплота парообразования - это физическая величина, которая показывает количество теплоты , нужное, чтобы превратить жидкость массой 1 кг в пар при температуре кипения. Обозначается удельная теплота парообразования буквой L. А единицей измерения является джоуль на килограмм (1 Дж/кг).
Удельную теплоту парообразования можно найти из формулы:
где Q - это количество теплоты,
m - масса тела.
Кстати, формула такая же, как и для расчета удельной теплоты плавления , разница лишь в обозначении. λ и L
Опытным путем найдены значения удельной теплоты парообразования различных веществ и составлены таблицы, откуда можно найти данные для каждого вещества. Так, удельная теплота парообразования воды равна 2,3*106 Дж/кг. Это означает, что на каждый килограмм воды необходимо потратить количество энергии, равное 2,3*106 Дж, чтобы превратить ее в пар. Но при этом вода должна уже обладать температурой кипения. Если вода изначально была более низкой температуры, то необходимо рассчитать еще то количество теплоты, которое потребуется для подогрева воды до ста градусов.
В реальных условиях часто требуется определить количество теплоты, необходимое для превращения в пар определенной массы какой-либо жидкости, поэтому чаще приходится иметь дело с формулой вида: Q=Lm, а значения удельной теплоты парообразования для конкретного вещества берут из готовых таблиц.
Всем известно, что вода в чайнике закипает при температуре 100 ˚С. Но обращали ли вы внимание, что температура воды в процессе кипения не меняется? Вопрос – куда девается образующаяся энергия, если мы постоянно держим емкость на огне? Она уходит на преобразование жидкости в пар. Таким образом, для перехода воды в газообразное состояние требуется постоянное поступление теплоты. То, сколько ее нужно для преобразования килограмма жидкости в пар такой же температуры, определяется физической величиной, которая называется удельная теплота парообразования воды.
Для кипения требуется энергия. Большая ее часть используется для разрыва химических связей между атомами и молекулами, в результате чего образуются пузырьки пара, а меньшая идет на расширение пара, то есть на то, чтобы образовавшиеся пузырьки могли лопнуть и выпустить его. Так как жидкость всю энергию вкладывает в переход в газообразное состояние, ее «силы» иссякают. Для постоянного возобновления энергии и продления кипения нужно подводить к емкости с жидкостью все новое и новое тепло. Обеспечить его приток может кипятильник, газовая горелка либо любой другой нагревательный прибор. Во время кипения температура жидкости не растет, идет процесс образования пара такой же температуры.
Разным жидкостям требуется разное количество теплоты для перехода в пар. Какое именно – показывает удельная теплота парообразования.
Понять, как определяется эта величина, можно из примера. Берем 1 л воды и доводим ее до кипения. Затем замеряем количество тепла, понадобившегося для выпаривания всей жидкости, и получаем значение удельной теплоты парообразования для воды. Для других химических соединений этот показатель будет другим.
В физике удельная теплота парообразования обозначается латинской буквой L. Измеряется она в джоулях на килограмм (Дж/кг). Вывести ее можно путем деления теплоты, израсходованной на испарение, на массу жидкости:
Данная величина очень важна для производственных процессов на основе современных технологий. Например, на нее ориентируются при производстве металлов. Оказалось, что если железо расплавить, а потом сконденсировать, при дальнейшем затвердении образуется более прочная кристаллическая решетка.
Значение удельной теплоты для различных веществ (r) определили в ходе лабораторных исследований. Вода при нормальном атмосферном давлении закипает при 100 °C, а теплота испарения воды составляет 2258,2 кДж/кг. Данный показатель для некоторых других веществ приведен в таблице:
| Вещество | t кипения, °C | r, кДж/кг |
|---|---|---|
| Азот | -196 | 198 |
| Гелий | -268,94 | 20,6 |
| Водород | -253 | 454 |
| Кислород | -183 | 213 |
| Углерод | 4350 | 50000 |
| Фосфор | 280 | 400 |
| Метан | -162 | 510 |
| Пентан | 36 | 360 |
| Железо | 2735 | 6340 |
| Медь | 2590 | 4790 |
| Олово | 2430 | 2450 |
| Свинец | 1750 | 8600 |
| Цинк | 907 | 1755 |
| Ртуть | 357 | 285 |
| Золото | 2 700 | 1 650 |
| Этиловый спирт | 78 | 840 |
| Метиловый спирт | 65 | 1100 |
| Хлороформ | 61 | 279 |
Однако этот показатель может изменяться под действием определенных факторов:
| t, °C | r, кДж/кг |
|---|---|
| 2500 | |
| 10 | 2477 |
| 20 | 2453 |
| 50 | 2380 |
| 80 | 2308 |
| 100 | 2258 |
| 200 | 1940 |
| 300 | 1405 |
| 374 | 115 |
| 374,15 |
| p, Па | t кип., °C | r, кДж/кг |
|---|---|---|
| 0,0123 | 10 | 2477 |
| 0,1234 | 50 | 2380 |
| 1 | 100 | 2258 |
| 2 | 120 | 2202 |
| 5 | 152 | 2014 |
| 10 | 180 | 1889 |
| 20 | 112 | 1638 |
| 50 | 264 | 1638 |
| 100 | 311 | 1316 |
| 200 | 366 | 585 |
| 220 | 373,7 | 184,8 |
| Критическое 221,29 | 374,15 | - |
Физики выяснили, что на обратный испарению процесс – конденсацию – пар тратит ровно столько же энергии, сколько пошло на его образование. Это наблюдение подтверждает закон сохранения энергии.
В противном случае было бы возможно создание установки, в которой жидкость испарялась бы, а потом конденсировалась. Разница между теплотой, необходимой для испарения, и теплотой, достаточной для конденсации, приводила бы к накоплению энергии, которая могла бы быть использована для других целей. По сути, был бы создан вечный двигатель. Но это противоречит физическим законам, а значит, невозможно.
Кипение, как мы видели, тоже испарение, только сопровождается оно быстрым образованием и ростом пузырьков пара. Очевидно, что во время кипения необходимо подводить к жидкости определённое количество теплоты. Это количество теплоты идёт на образование пара. Причём различные жидкости одной и той же массы требуют разное количество теплоты для обращения их в пар при температуре кипения.
Опытами было установлено, что для испарения воды массой 1 кг при температуре 100 °С требуется 2,3 10 6 Дж энергии. Для испарения эфира массой 1 кг, взятого при температуре 35 °С, необходимо 0,4 10 6 Дж энергии.
Следовательно, чтобы температура испаряющейся жидкости не изменялась, к жидкости необходимо подводить определённое количество теплоты.
Физическая величина, показывающая, какое количество теплоты необходимо, чтобы обратить жидкость массой 1 кг в пар без изменения температуры, называется удельной теплотой парообразования.
Удельную теплоту парообразования обозначают буквой L. Её единица - 1 Дж/кг.
Опытами установлено, что удельная теплота парообразования воды при 100 °С равна 2,3 10 6 Дж/кг. Иными словами, для превращения воды массой 1 кг в пар при температуре 100 °С требуется 2,3 10 6 Дж энергии. Следовательно, при температуре кипения внутренняя энергия вещества в парообразном состоянии больше внутренней энергии такой же массы вещества в жидком состоянии.
Таблица 6.
Удельная теплота парообразования некоторых веществ (при температуре кипения и нормальном атмосферном давлении)
Соприкасаясь с холодным предметом, водяной пар конденсируется (рис. 25). При этом выделяется энергия, поглощённая при образовании пара. Точные опыты показывают, что, конденсируясь, пар отдаёт то количество энергии, которое пошло на его образование.

Рис. 25. Конденсация пара
Следовательно, при превращении 1 кг водяного пара при температуре 100 °С в воду той же температуры выделяется 2,3 10 6 Дж энергии. Как видно из сравнения с другими веществами (табл. 6), эта энергия довольно велика.
Освобождающаяся при конденсации пара энергия может быть использована. На крупных тепловых электростанциях отработавшим в турбинах паром нагревают воду.
Нагретую таким образом воду используют для отопления зданий, в банях, прачечных и для других бытовых нужд.
Чтобы вычислить количество теплоты Q, необходимое для превращения в пар жидкости любой массы, взятой при температуре кипения, нужно удельную теплоту парообразования L умножить на массу m:
Из этой формулы можно определить, что
m = Q / L, L = Q / m
Количество теплоты, которое выделяет пар массой т, конденсируясь при температуре кипения, определяется по той же формуле.
Пример . Какое количество энергии требуется для превращения воды массой 2 кг, взятой при температуре 20 °С, в пар? Запишем условие задачи и решим её.

Явление превращения вещества из жидкого состояния в газообразное называется парообразованием . Парообразование может осуществляться в виде двух процессов: и.
Второй процесс парообразования - кипение. Наблюдать этот процесс можно с помощью простого опыта, нагревая воду в стеклянной колбе. При нагревании воды в ней через некоторое время появляются пузырьки, в которых содержатся воздух и насыщенный водяной пар, который образуется при испарении воды внутри пузырьков. При повышении температуры давление внутри пузырьков растёт, и под действием выталкивающей силы они поднимаются вверх. Однако, поскольку температура верхних слоёв воды меньше, чем нижних, пар в пузырьках начинает конденсироваться, и они сжимаются. Когда вода прогреется по всему объёму, пузырьки с паром поднимаются до поверхности, лопаются, и пар выходит наружу. Вода кипит. Это происходит при такой температуре, при которой давление насыщенного пара в пузырьках равно атмосферному давлению.
Процесс парообразования, происходящий во всем объёме жидкости при определённой температуре, называют . Температуру, при которой жидкость кипит, называют температурой кипения .
Эта температура зависит от атмосферного давления. При повышении атмосферного давления температура кипения возрастает.
Опыт показывает, что в процессе кипения температура жидкости не изменяется, несмотря на то, что извне поступает энергия. Переход жидкости в газообразное состояние при температуре кипения связан с увеличением расстояния между молекулами и соответственно с преодолением притяжения между ними. На совершение работы по преодолению сил притяжения расходуется подводимая к жидкости энергия. Так происходит до тех пор, пока вся жидкость не превратится в пар. Поскольку жидкость и пар в процессе кипения имеют одинаковую температуру, то средняя кинетическая энергия молекул не изменяется, увеличивается лишь их потенциальная энергия.
На рисунке приведён график зависимости температуры воды от времени в процессе её нагревания от комнатной температуры до температуры кипения (АВ), кипения (ВС), нагревания пара (CD), охлаждения пара (DE), конденсации (EF) и последующего охлаждения (FG).
Для превращения разных веществ из жидкого состояния в газообразное требуется разная энергия, эта энергия характеризуется величиной, называемой удельной теплотой парообразования.
Удельная теплота парообразования (L ) — это величина, равная отношению количества теплоты, которое нужно сообщить веществу массой 1 кг, для превращения его из жидкого состояния в газообразное при температуре кипения.
Единица удельной теплоты парообразования - [L ] = Дж/кг.
Чтобы рассчитать количество теплоты Q, которое необходимо сообщить веществу массой тп для его превращения из жидкого состояния в газообразное, необходимо удельную теплоту парообразования (L ) умножить на массу вещества: Q = Lm.
При конденсации пара выделяется некоторое количество теплоты, причем его значение равно значению количества теплоты, которое необходимо затратить для превращения жидкости в пар при той же температуре.